Lungekreft (bronkialkarsinom) er en av de vanligste kreftformene i Tyskland. Den viktigste risikofaktoren er røyking. Passiv røyking kan også føre til lungekreft. Den ondartede svulsten kan behandles på en rekke måter, inkludert cellegift og kirurgi. Likevel er lungekreft sjelden kurbar. Les all viktig informasjon om lungekreft her!
Lungekreft: kort oversikt
- symptomer: til å begynne med ofte ingen eller bare uspesifikke symptomer som vedvarende hoste, brystsmerter og tretthet. Senere kan symptomer som kortpustethet, mild feber, alvorlig vekttap og blodig sputum tilføres.
- Hovedformer for lungekreft: Vanligst er ikke-småcellet lungekreft (med adenokarsinom, plateepitelkarsinom osv.). Mindre vanlig, men mer aggressiv, er småcellet lungekreft.
- årsaker: Spesielt røyking. Andre risikofaktorer inkluderer asbest, arsenforbindelser, radon, et høyt nivå av miljøgifter i luften og et lite vitamin kosthold.
- undersøkelser: Røntgen fra brystet (røntgen fra brystet), computertomografi (CT), MR (magnetisk resonansavbildning, MR), undersøkelse av vevsprøver (biopsier), positronemisjonstomografi (vanligvis i kombinasjon med CT som FDG-PET / CT), blodprøver, undersøkelse utstøting, undersøkelse av «lungevannet» (pleural funksjon)
- Behandlingsmuligheter: Kirurgi, strålebehandling, cellegift.
- prognose: Lungekreft gjenkjennes vanligvis sent og er derfor sjelden herdbar.
Lungekreft: tegn
Lungekreft (lungekarsinom) forårsaker til å begynne med ofte ingen eller bare ikke-spesifikke klager, Disse inkluderer trøtthet, hoste eller Brystsmerter, Men slike klager kan også ha mange andre årsaker, for eksempel forkjølelse eller bronkitt. Derfor gjenkjennes ofte ikke lungekreft i tidlige stadier. Det gjør terapien vanskeligere.
Mer uttalte tegn forårsaker lungekreft når den allerede er avansert. Så, for eksempel Raskt vekttap, blodig sputum og kortpustethet oppstå.
Har lungekreft allerede slektninger til datter (metastaser) dannet i andre deler av kroppen kommer stort sett andre symptomer lagt til. For eksempel kan metastaser i hjernen skade nervene. Mulige konsekvenser inkluderer hodepine, kvalme, syns- og balanseforstyrrelser eller til og med lammelse. Hvis kreftcellene har angrepet beinene, kan artroselignende smerte oppstå.
Les mer om de forskjellige tegnene på lungekreft i artikkelen Lungekreft: symptomer.
Lungekreft: stadier
Som enhver kreft forekommer lungekreft fordi celler degenererer. I dette tilfellet er de celler i lungevevet. De degenererte cellene formerer seg ukontrollert og fortrenger sunt vev i miljøet. Senere kan individuelle kreftceller spre seg gjennom blodet og lymfekarene i kroppen. Ofte danner de da en sekundær svulst (metastase) andre steder.
En lungekreft sykdom kan være så langt avansert. For eksempel snakker man om et tidlig stadium eller i verste fall om lungekreftens sluttstadium. Men dette er ikke nøyaktig definerte begrep. Av denne grunn bruker leger vanligvis den såkalte TNM-klassifiseringen: den gjør det mulig å beskrive de individuelle lungekreftene nøyaktig. Dette er viktig, fordi behandlingen og forventet levealder for en pasient er avhengig av det respektive lungekreftstadiet.
Lungekreft: TNM-klassifisering og stadier
TNM-ordningen er et internasjonalt system for å beskrive spredningen av en svulst. Det står:
- «T» for størrelsen på Tumors
- «N» for mulig involvering av lymfeknuter (Nodi lymfatiske)
- «M» for mulig tilstedeværelse av Metastasen
For hver av disse tre kategoriene tildeler du en numerisk verdi. Det indikerer hvor avansert kreft hos en pasient er.
Den eksakte TNM-klassifiseringen for lungekreft er kompleks. Følgende tabell gir en grov oversikt:
|
TNM |
Tumorkarakter ved diagnose |
erklæring |
|
TX |
Okkult (skjult) karsinom |
Verken røntgenbilder eller computertomografi (CT) kan oppdage en svulst, men sputumet til pasienten har kreftceller. |
|
T1 |
Svulsten er mindre enn 3 cm. Hovedbronkiene påvirkes ikke. |
De viktigste bronkiene er de første grenene av luftrøret i lungene. |
|
T2 |
Svulsten har en størrelse på 3 til 5 cm (T2a) eller 5 til 7 cm (T2b) |
og / eller minst ett av følgende kriterier er gitt:
|
|
T3 |
Svulsten er større enn 7 cm |
eller gitt minst ett av følgende kriterier:
|
|
T4 |
Tumorstørrelse spiller ikke lenger en rolle her, i stedet er dette stadiet til stede når
|
|
|
N0 |
ingen lymfeknuter involvering |
|
|
N1 |
Ipsilaterale lymfeknuter involvering rundt bronkiene (peribronchial) eller ved inntreden av lungekarene og hovedbronkiene i lungene (hilar) |
Begrepet «ipsilateral» betyr at den berørte lymfeknuten er i samme lunge eller halvparten av kroppen som den forårsakende lungetumoren. «Contralateral» betyr at lymfeknuter i den andre halvparten av kroppen / lungen påvirkes. |
|
N2 |
Ipsilateral lymfeknute involvering under forgreningen av hovedbronkiene (subkarinal) eller brysthulen mellom de to lungene (mediastinal) |
|
|
N2 |
Ipsilateral lymfeknuter involvering over clavicle (supraklavikulær) eller nakke eller angrep (minst) av en kontralateral lymfeknute |
|
|
M0 |
Ingen fjerne metastaser |
|
|
M1A |
Metastaser i den kontralaterale lunge og / eller tung involvering av lungefôret og / eller kreftcellene i effusjonsvæsken i lungefôret er påviselige |
|
|
M1B |
fjernmetastaser |
Fjernmetastaser påvirker vanligvis leveren, hjernen, bein og binyrene |
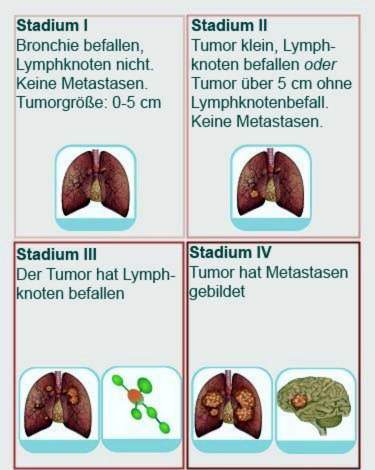
TNM-klassifiseringen bestemmer lungekreftstadiet: 4 stadier skilles. Jo høyere stadium, jo mer avansert sykdom:
Lungekreftstadium I
Dette stadiet er delt inn i A og B. Fase IA tilsvarer en klassifisering av T1 N0 M0. Det vil si: Den ondartede lungetumoren er mindre enn tre centimeter. Hovedbronkiene påvirkes ikke av kreften. I tillegg påvirkes ingen lymfeknuter og det har ennå ikke dannet noen fjerne metastaser.
I stadium IB har svulsten en klassifisering av T2a N0 M0: den er tre til fem centimeter i størrelse og begrenset til lungene. Svulsten har derfor verken påvirket lymfeknuter eller spredt seg i andre organer eller vev.
I dette første stadiet har lungekreft den beste prognosen og er ofte kurerbar.
Lungekreftfase II
Også her er A og B. differensiert.Fase IIA inkluderer lungesvulster i T2b-kategorien, som ennå ikke har påvirket lymfeknuter (N0) eller har dannet metastaser (M0). Her hører også svulster i kategorien T1 N1 M0.
Fase IIB inkluderer svulster i klassifiseringen T3 N0 M0 eller T2b N1 M0.
Selv i stadium II er lungekreft fremdeles helbredelig i noen tilfeller. Forventet levealder for pasienter er allerede lavere enn i stadium I.
Lungekreft stadium III
Fase IIIA er når lungekreft er klassifisert som T1 / T2 N2 M0 eller T3 N1 / 2 M0 eller T4 N0 M0. Fase IIIB beskriver hver lungekreft med N3 M0 eller T4 N2 M0.
I lungekreftstadium III har svulsten kommet så langt at pasienter bare kan bli kurert i sjeldne tilfeller.
Lungekreft stadium IV
Levealder og sjanser for bedring er veldig lave på dette stadiet. Pasienten kan bare få palliativ terapi: den tar sikte på å lindre symptomene og forlenge overlevelsen. Fase IV inkluderer hver lungekreft som allerede har dannet fjerne metastaser (M1). Tumorstørrelse og involvering av lymfeknuter spiller ikke lenger en rolle – de kan variere.
Litencelle bronkialkarsinom: alternativ klassifisering
Leger skiller to hovedgrupper av lungekreft: småcellet lungekarsinom og ikke-småcellet lungekreft (se nedenfor). Begge kan klassifiseres i henhold til ovennevnte TNM-klassifisering på stadioner.
For småcellet bronkialkarsinom kan en annen alternativ klassifisering alternativt brukes:
- veldig begrenset sykdom: maksimalt opp til T2 og N1
- begrenset sykdom: T3 / 4 med N0 / 1 eller T1 til T4 med N2 / N3
- omfattende sykdom: M1 uavhengig av T og N
Lungekreft: behandling
Terapien mot et bronkialkarsinom er veldig komplisert. Den er individuelt tilpasset hver pasient: For det første avhenger det av lungekreftens type og spredning. Imidlertid spiller pasientens alder og generelle helse også en viktig rolle i terapiplanleggingen.
Hvis behandlingen tar sikte på å kurere lungekreft, kalles det en kurativ terapi, Pasienter som ikke lenger er i stand til å lege, får en palliativ terapi, Det er ment å maksimere pasientens levetid og lindre symptomene hans.
Leger fra forskjellige sykehusdisipliner gir hverandre råd om den endelige behandlingsstrategien. Disse inkluderer for eksempel radiologer, kirurger, internister, strålingsleger og patologer. I vanlige økter («tumorboards») prøver de å finne den beste lungekreftterapien for en pasient.
Det er tre forskjellige terapeutiske tilnærminger, som brukes enkeltvis eller i kombinasjon:
- en operasjon for å fjerne svulsten
- cellegift med spesielle medisiner mot kreftceller
- strålingen av svulsten
Lungekreft: kirurgi
En reell sjanse for bedring ved lungekreft vanligvis bare så lenge du kan operere. Kirurgen prøver å fjerne det kreftformede lungevevet fullstendig. Han kutter også ut en kant med sunt vev. Så han vil sørge for at ingen kreftceller blir igjen. Avhengig av spredning av bronkialkarsinom, kan du enten fjerne det en eller to lungelobber (Lobektomi, bilobektomi) eller til og med en hel lunge (Pneumonektomi).
I noen tilfeller vil det være fornuftig å ta ut en hel lunge. Pasientens dårlige helse tillater ikke dette. Da fjerner kirurgen så mye som nødvendig, men så lite som mulig.
I operasjonen, omkringliggende lymfeknuter kuttet ut (mediastinal lymfeknuter disseksjon). Dette gjøres selv om de foreløpige undersøkelsene ikke har gitt noen indikasjon på kreftinvolvering av lymfeknuter. Ofte er dette den første stasjonen for å flytte, som ikke kan gjenkjennes i begynnelsen.
Dessverre er det ofte ingen sjanse for at en operasjon kan kurere lungekreft: svulsten er allerede for avansert. Hos andre pasienter ville svulsten i prinsippet være operabel. Imidlertid er lungefunksjonen til pasienten så dårlig at han ikke ville være i stand til å takle å fjerne deler av lungene. I oppkjøringen sjekker legene derfor med spesielle undersøkelser om en operasjon på en pasient gir mening.
Lungekreft: cellegift
Som mange andre kreftformer, kan lungekreft også behandles med cellegift. Pasienten får medisiner som hemmer celledeling og dermed tumorvekst. Disse midlene kalles kjemoterapeutiske midler eller cytostatika.
Cellegift alene er ikke nok til å kurere lungekreft. De brukes derfor vanligvis i kombinasjon med andre behandlinger. For eksempel kan det gjøres før operasjon for å krympe svulsten (Neoadjuvant cellegift). Da må kirurgen kutte ut mindre vev.
I andre tilfeller antas cellegift etter operasjon å ødelegge kreftceller som fremdeles er i kroppen (adjuvant cellegift).
Kjemoterapi for lungekreft eksisterer vanligvis flere behandlingssykluser, Så det er visse dager når legen administrerer medisinen. Innimellom tas to til tre ukers behandlingspauser. Stort sett mottar pasienten medisinene som en infusjon via en blodåre. Noen ganger er imidlertid preparatene også gitt i tablettform (muntlig).
For å sjekke effekten av cellegift blir pasienten regelmessig undersøkt ved hjelp av computertomografi (CT). Så legen erkjenner om han må justere cellegift. Han kan for eksempel øke medisindosen eller foreskrive et annet cytostatisk medikament.
Lungekreft: stråling
En annen tilnærming til behandling av lungekreft er stråling. Lungekreftpasienter får vanligvis strålebehandling i tillegg til en annen behandlingsform. Som cellegift kan stråling være for eksempel før eller etter operasjonen gjort. Ofte brukes de også i tillegg til cellegift. Det er det du kaller det kjemoradioterapi.
Noen lungekreftpasienter får også en såkalt Profylaktisk kraniell bestråling, Med andre ord blir hodeskallen bestrålt som en forholdsregel for å forhindre dannelse av hjernemetastaser.
Hvis lungekreft fremdeles er på et veldig tidlig stadium, er bestråling noen ganger tilstrekkelig som den eneste behandlingen for å kurere pasienten.
Andre behandlinger mot lungekreft
De nevnte terapiene er rettet direkte mot den primære svulsten og mulige lungekreftmetastaser. I løpet av sykdommen kan det imidlertid oppstå forskjellige klager og komplikasjoner, som også må behandles:
- Når det er en effusjon mellom lungene og lungenpleuravæske), det suger ham av (Pleurapunktion). Hvis effusjonen fortsetter igjen, kan du sette inn et lite rør mellom lunge og pleura, som væsken strømmer over. Han holder seg lenger i kroppen (drenering av brystet).
- Svulsten kan Blødning i bronkiene forårsake. Disse kan stoppes, for eksempel ved selektiv lukking av det aktuelle blodkar, for eksempel som en del av en bronkoskopi.
- Den voksende svulsten kan Lukk blodkar eller luftveier, For å få det gjennom igjen, kan du sette inn en stent, så et stabiliserende rør. I andre tilfeller fjernes tumorvevet på det aktuelle stedet, for eksempel med en laser.
- Avansert lungekreft kan forårsake sterke smerter (kreftsmerterÅrsaken). Pasienten får deretter en passende smerteterapi, for eksempel smertestillende som en tablett eller sprøyte. For smertefulle benmetastaser kan stråling gi lettelse.
- pustevansker kan lettes med medisiner og oksygen. Nyttig er også spesielle pusteteknikker og riktig lagring av pasienten.
- ved tungt vekttap kan det hende du må mate pasienten kunstig.
- Bivirkninger av cellegift som kvalme og anemi kan behandles med passende medisiner.
I tillegg til behandling av fysiske plager, er det også veldig viktig at pasienten mentalt godt ivaretatt er. Psykologer, sosiale tjenester og selvhjelpsgrupper hjelper til med sykdomshåndtering. Dette øker livskvaliteten til pasienten. De pårørende kan og bør inkluderes i terapikonseptene.
Litencelle bronkialkarsinom
Behandlingen av lungekreft påvirkes av hvilken type svulst det er. Avhengig av hvilke celler i lungevevet til kreftceller, skiller leger to hovedgrupper av lungekreft: En av dem er småcellet lungekreft (SCLC = litencellet lungekreft).
Denne typen lungekreft vokser veldig raskt og danner tidlige metastaser (metastaser) i andre deler av kroppen. Derfor er cellegift den viktigste behandlingen her. Mange pasienter får også strålebehandling. Dette bør forbedre sjansene for suksess for behandlingen.
Kirurgi gir vanligvis bare mening hvis svulsten fremdeles er veldig liten og ingen eller bare noen få nærliggende lymfeknuter er berørt. Dette gjelder imidlertid bare individuelle pasienter: på diagnosetidspunktet er vanligvis småcellet lungekreft mer avansert.
Les mer om utviklingen, behandlingen og prognosen for denne formen for lungekreft i artikkelen SCLC: Small Cell Lung Cancer.
Ikke-småcellet lungekarsinom
Ikke-småcellet lungekreft er den vanligste formen for lungekreft. Det er ofte forkortet til NSCLC («ikke-småcellet lungekreft»). Strengt tatt omfatter begrepet «ikke-småcelle bronkialkarsinom» forskjellige typer svulster. Disse inkluderer for eksempel adenokarsinom og plateepitelkarsinom.
For alle ikke-småcellet lungekarsinomer vokser de saktere enn småcellet lungekreft og senere formmetastaser. De reagerer ikke så bra på cellegift.
Valgfri behandling er derfor, hvis mulig, en operasjon: kirurgen prøver å fjerne svulsten fullstendig. Hvis dette ikke er mulig, mottar pasienten ekstra stråling. Før eller etter operasjonen kan cellegift gis som støtte. Hvis ikke-småcellet lungekarsinom oppdages på et veldig tidlig stadium, kan til og med enkelteksponering være tilstrekkelig.
I noen tid har det vært andre terapeutiske tilnærminger som behandling med antistoffer. De er bare egnet for visse pasienter.
Les mer om denne utbredte formen for lungekreft i artikkelen NSCLC: Non-Small Cell Lung Cancer.
Lungekreft: årsaker og risikofaktorer
Årsaken til lungekreft er en ukontrollert vekst av celler i det såkalte bronkialsystemet. Dette refererer til de store og små luftveiene i lungene (bronkier og bronkioler). Det medisinske navnet for lungekreft er derfor bronkialkarsinom. Ordet del «karsinom» står for en ondartet svulst fra såkalte epitelceller. De danner omslagsstoffet som fører luftveiene.
De ukontrollerte voksende cellene formerer seg veldig raskt. Debei fortrenger i økende grad sunt lungevev. I tillegg kan kreftcellene spre seg gjennom blod og lymfekar og danne en dattergulv andre steder. Slike fjerninger kalles lungekreftmetastaser.
Metastaser i lungekreft bør ikke forveksles med lungemetastaser: Dette er sekundære svulster i lungene som kommer fra kreftsvulster andre steder i kroppen. For eksempel forårsaker tykktarmskreft og nyrecellekarsinom ofte lungemetastaser.
Røyking: Den viktigste risikofaktoren
Den viktigste risikofaktoren for ukontrollert og ondartet cellevekst i lungene er røyke, Rundt 90 prosent av alle menn med lungekreft har aktivt røkt eller gjør det fortsatt. For kvinner gjelder dette minst 60 prosent av pasientene. Jo høyere risiko for sykdom, jo tidligere noen begynte å røyke og jo mer røyker.
Leger måler det tidligere sigarettforbruket av en pasient i enheten «pakke år«(Pakkeår). Hvis noen røyker en pakke sigaretter om dagen i ett år, regnes dette som «ett pakkeår». Hvis han røyker en boks om dagen i ti år eller to bokser om dagen i fem år, er det 10 pakke år hver. Jo flere år med emballasje, jo høyere er risikoen for lungekreft.
I tillegg til antall røykede sigaretter Type røyking en rolle: jo mer røyk du inhalerer, jo verre er det for lungene. Risikoen for lungekreft har også innvirkning sigaretter steder: Sterke eller til og med filterløse sigaretter er spesielt skadelige.
I noen år vet man det også Tenåringer og kvinner mer følsomme for kreftfremkallende stoffer i tobaksrøyk enn voksne og menn.
Imidlertid er det ikke alle som røykte noen år i fortiden deres, må være redd for lungekreft. Heldigvis kan lungene også komme seg. Bare noen få år etter røykeavvenning har risikoen for lungekreft falt synlig. Cirka 20 til 30 år etter den siste sigaretten har en eks-røyker omtrent samme sykdomsrisiko igjen som noen som aldri har slukket. Så det er aldri for sent å slutte å røyke.
Passiv røyking øker også risikoen for lungekreft!
Andre risikofaktorer for lungekreft
Bortsett fra å røyke, er det andre faktorer som kan øke risikoen for lungekreft:
- Materialer som Asbest, arsenforbindelser eller støv av kvarts og nikkel
- Høy forurensning av luft: Den viktigste faktoren er sot. Partikler virker også å ha en negativ innvirkning på lungekreftrisikoen.
- radon: Naturlig, radioaktiv gass konsentreres i visse områder. Det finnes hovedsakelig i underetasjer i bygninger.
- Gene: I en viss grad ser lungekreft ut til å være arvelig. Spesielt hos veldig unge pasienter mistenker eksperter en genetisk disposisjon. Dette kan gjøre menneskene mer utsatt for lungeskadelige påvirkninger (som røyking).
- Lunge arrdannelse: De oppstår for eksempel som et resultat av tuberkulose eller etter operasjon.
- virus: Virussykdommer kan også være involvert i utviklingen av bronkialkreft. HIV og humane papillomavirus (HPV) mistenkes.
- Kosthold med lite vitamin: Hvis du spiser lite frukt og grønnsaker, ser det ut til at kreften i lungekreft øker. Dette gjelder spesielt for røykere. Inntaket av vitamintilskudd er imidlertid ikke et alternativ: Spesielt med røykere ser det ut til at slike preparater øker risikoen for bronkialkreft ytterligere.
Hvis flere av disse faktorene er til stede samtidig, legger sannsynligheten for lungekreft ikke bare opp: Snarere øker risikoen for sykdom mange ganger over. For eksempel øker en høy forurensningsbelastning i luften lungekreftrisikoen hos røykere mye mer enn hos ikke-røykere.
Noen ganger kan du gjøre det ingen årsak til lungekreft finne. Dette kalles en idiopatisk sykdom. Av alle typer lungekreft gjelder dette oftest det såkalte adenokarsinom. Dette er en form for ikke-småcellet lungekarsinom.
Lungekreft: undersøkelser og diagnose
Diagnosen lungekreft stilles ofte sent. Symptomer som vedvarende hoste, brystsmerter og kortpustethet blir ofte ikke anerkjent av røykere som mulige tegn på lungekreft. De fleste pasienter klandrer rett og slett røyking. Andre mistenker alvorlig forkjølelse, bronkitt eller lungebetennelse bak ubehaget. Bare medisinske undersøkelser gir deretter mistanke om bronkialkarsinom.
Det første kontaktpunktet for mulige symptomer på lungekreft er familielegen. Om nødvendig vil han henvise pasienten til spesialister, for eksempel til en røntgenspesialist (radiolog), pulmonolog (pulmonolog) eller kreftspesialist (onkolog). For å diagnostisere lungekreft er det nødvendig med en undersøkelse av sykehistorien, en fysisk undersøkelse og forskjellige apparater.
Sykehistorie og fysisk undersøkelse
Først samler legen pasientens sykehistorie (anamnese) i samtale med pasienten:
Han beskriver symptomene som luftveisnød eller smerter i brystet nøyaktig. Han spør også om risikofaktorer for lungekreft, for eksempel spør han om pasienten røyker eller jobber med materialer som asbest eller arsenforbindelser.
Informasjon om mulige eksisterende eller underliggende sykdommer som KOLS eller kronisk bronkitt er også viktig for diagnosen lungekreft. Pasientene bør også fortelle legen om det allerede var tilfeller av lungekreft i familien.
Etter anamneseintervjuet vil legen nøye undersøke pasienten fysisk. For eksempel tapper han og hører lungene til pasienten og måler blodtrykket og pulsen. Etterforskningen kan gi mulige ledetråder til årsaken til klagene. I tillegg kan legen dermed bedre vurdere den generelle helsen til pasienten.
Røntgen
Ved å bruke en røntgen av brystet (røntgen på brystet), kan legen allerede oppdage visse endringer i lungevevet. Hvis dette fører til mistanke om lungekreft, er neste trinn datastomografi (CT).
For øvrig undersøker legen pasienten i to nivåer, dvs. fra fronten og fra siden.
Computertomografi (CT)
Computertomografi gir detaljerte snittbilder av lungene i høy oppløsning. Dette er mulig ved hjelp av røntgenstråler, som er betydelig høyere dose enn ved vanlig røntgen. I tillegg får pasienten et kontrastmiddel på forhånd. Så de forskjellige vevsstrukturene er bedre representert.
Legen kan bruke CT for å vurdere mistenkelige lungeforandringer bedre enn røntgenbildene. Dette kan bekrefte mistanken om lungekreft.
Undersøkelse av vevsprøver (biopsi)
For å være sikker på at et fremtredende sted i lungevevet faktisk er et bronkialkarsinom, må man ta et lite stykke vev og undersøke det mikroskopisk. Avhengig av hvor det mistenkelige området befinner seg, brukes forskjellige metoder:
I lungerefleksjonen (bronkoskopi) introduserer et rør med et lite kamera (endoskop) over munnen eller nesen i luftrøret til pasienten og videre inn i bronkiene. Når man ser på innsiden, kan en svulst ofte allerede gjenkjennes visuelt. I tillegg kan legen i forbindelse med bronkoskopi med fine instrumenter under visuell kontroll vevsprøver og sekresjoner fra lungene.
Hvis du ikke kan nå det mistenkelige vevet gjennom bronkiene dårlig eller ikke i det hele tatt, utfører legen en såkalt transthoracic nål aspirasjon Gjennom: Han stikker med en veldig fin nål fra utsiden mellom ribbeina. Under CT-kontroll fører han nålspissen til det mistenkte lungeområdet. Han suger deretter (aspirerer) litt vev over nålen.
Hos noen pasienter er verken bronkoskopi eller transthorakisk nålaspirasjon mulig. I andre tilfeller gir begge studiene ikke noe klart resultat. Da kan man kirurgisk biopsi nødvendig: enten åpner kirurgen brystkassen med et større snitt (thoracotomy) og tar en prøve av det mistenkelige vevet. Eller han legger små kutt i brystet, som han introduserer et lite kamera og fine instrumenter for vevsfjerning (videoassistert thorakoskopi, VATS).
Den fjernede vevsprøven undersøkes under mikroskopet. Som regel er det allerede mulig å påvise ved hjelp av færre celler om lungekreft er til stede og i så fall hvilken type tumor (cytologisk diagnose). Bare i spesielle tilfeller er det nødvendig å undersøke større vevssnitt (histologisk diagnose).
Undersøkelse av tumorspredning (iscenesettelse)
Hvis diagnosen «lungekreft» er klar, er neste trinn å undersøke dens spredning i kroppen. Denne delen av studien omtales av leger som iscenesettelse (engelsk for «iscenesettelse»). Bare ved en slik iscenesettelse kan de klassifisere bronkialkarsinom i henhold til TNM-klassifiseringen.
Iscenesettelse involverer tre trinn:
- Undersøkelse av tumorstørrelse (T-status)
- Undersøkelse av lymfeknuteinvolvering (N-status)
- Søk etter metastaser (M-status)
Undersøkelse av den primære svulsten (T-status)
Først av alt undersøker vi størrelsen på svulsten som lungekreft stammer fra (primær tumor). For dette formålet mottar pasienten et kontrastmiddel før han bruker brystet og øvre del av magen computertomografi (CT) undersøkt. Kontrastmediet akkumuleres i kort tid hovedsakelig i tumorvevet og forårsaker et merke på CT-bildet. Så legen kan vurdere omfanget av den primære svulsten.
Hvis undersøkelsen med CT ikke er meningsfull nok, brukes ytterligere prosedyrer. Dette kan være f.ekse Ultralydundersøkelse i brystet (thorax sonography) eller en MR Vær (MRT).
Undersøkelse av lymfeknuteinvolvering (N-status)
For å planlegge behandlingen optimalt, må legen vite om lungekreft allerede har påvirket lymfeknuter. Igjen hjelper undersøkelsen ved hjelp av computertomografi (CT). Ofte brukes en spesiell teknikk: den såkalte FDG-PET / CT, Dette er en kombinasjon av positron emission tomography (PET) og CT:
Positronemisjonstomografi (PET) er en nukleærmedisinsk undersøkelse. Den liggende pasienten injiseres først en ørliten mengde radioaktivt stoff i en blodåre. FDG-PET / CT handler om FDG, Dette er et radiomerket enkel sukker (fluorodeoxyglucose). Det sprer seg i kroppen og akkumuleres spesielt i vev med økt metabolsk aktivitet, for eksempel i kreftvev. I løpet av denne tiden må pasienten være så stille som mulig. Etter omtrent 45 (til 90) minutter blir PET / CT-skanningen utført for å visualisere fordelingen av FDG i kroppen:
PET-kameraet kan meget godt representere den forskjellige metabolske aktiviteten i de forskjellige vevene. Spesielt aktive områder (som kreftceller i lymfeknuter eller metastaser) «lyser» bokstavelig talt på PET-bildet. Ben, organer og andre strukturer i kroppen kan ikke representere PET så bra. Dette gjøres av den nesten samtidig datatomografien CT (PET-kamera og CT er kombinert i en enhet). Det gir en veldig nøyaktig fremstilling av de forskjellige anatomiske strukturer. Kombinert med den nøyaktige kartleggingen av metabolsk aktivitet, er det mulig å lokalisere kreftsykdommer.
Konklusjon: Ved bruk av FDG-PET / CT kan metastaser av lungekreft i lymfeknuter og enda fjernere organer og vev vises veldig nøyaktig. For å være på den sikre siden, kan legen ta en vevsprøve av det mistenkelige området og undersøke det for kreftceller (biopsi).
Søk etter metastaser (M-status)
Das Streuen von Krebszellen in andere Organe ist ein großes Problem beim Bronchialkarzinom. Metastasen bilden sich besonders oft in Leber und Gehirn sowie in den Knochen und Nebennieren. Prinzipiell kann aber jede Körperstruktur von den Krebszellen befallen werden. Lungenkrebs, der bereits gestreut hat, gilt als nicht mehr heilbar.
Mit der oben beschriebenen Spezialuntersuchung FDG-PET/CT können Metastasen überall im Körper nachgewiesen werden. Um mögliche Absiedlungen im Gehirn ausfindig zu machen, wird zudem der Schädel mittels MR (MRT) untersucht.
Bei manchen Patienten ist eine FDG-PET/CT nicht möglich. Die Alternative ist dann eine computertomografi eller Ultraschall-Untersuchung des Rumpfes und zusätzlich eine sogenannte Knochenszintigrafie, også Ganzkörper-MRT-Aufnahmen sind möglich.
Blutuntersuchungen
Es gibt keine Blutwerte, mit deren Hilfe sich Lungenkrebs sicher diagnostizieren lässt. Allerdings kann man sogenannte Tumormarker im Blut bestimmen. Das sind Substanzen, deren Blutspiegel bei einer Kresberkrankung erhöht sein kann. Denn die Tumormarker werden entweder von den Krebszellen selbst oder aber vom Körper als Reaktion auf den Krebs verstärkt produziert.
Mediziner kennen zwei Tumormarker, die bei Lungenkrebs oft erhöht sind: die neuronenspezifische Enolase (NSE) und CYFRA 21-1. Anhand dieser Marker allein kann man aber keine Diagnose stellen. Sie dienen vielmehr der Verlaufsbeurteilung: Ihre Konzentration im Blut wird regelmäßig bestimmt. So kann der Arzt abschätzen, wie schnell der Tumor wächst beziehungsweise ob nach einer Behandlung erneut Krebszellen auftauchen.
Untersuchung des Auswurfs
Der Auswurf (Sputum), den ein Patient aus der Lunge hochhustet, kann ebenfalls untersucht werden. Diese Methode wird vor allem dann angewendet, wenn andere Diagnoseverfahren nicht möglich sind (etwa weil der Gesundheitszustand des Patienten zu schlecht ist).
Ist der Auswurf unauffällig, heißt das aber nicht unbedingt, dass kein Lungenkrebs vorliegt. Die Untersuchung des Auswurfs dient eher dazu, einen bereits vorhandenen Verdacht zu bestätigen.
Untersuchung von Lungenwasser
Bei Lungenkrebs-Patienten bildet sich oft «Lungenwasser». Das heißt: Es sammelt sich vermehrt Flüssigkeit zwischen Lungenfell und Rippenfell. Ein solcher Pleuraerguss kann aber auch andere Ursachen haben. Zur Abklärung wird der Arzt über eine feine Hohlnadel eine Probe des Ergusses entnehmen (Pleurapunktion) und mikroskopisch untersuchen. So kann er feststellen, wodurch der Erguss entstanden ist.
Gibt es Vorsorgeuntersuchungen bei Lungenkrebs?
Eine allgemeine Früherkennung, wie man sie zum Beispiel bei Brustkrebs, Darmkrebs oder Hautkrebs anwendet, ist bei Lungenkrebs schwierig. Man könnte zwar regelmäßig zum Beispiel Röntgen-Aufnahmen des Brustkorbs machen, das Blut auf Tumormarker untersuchen oder den Auswurf analysieren. Solche Vorsorgeuntersuchungen sind aber entweder zu ungenau oder aber zu empfindlich. Im zweiten Fall könnte sich ein unbegründeter Krebsverdacht ergeben. Außerdem bedeuten regelmäßige Röntgen- oder auch CT-Untersuchungen eine Strahlenbelastung für den Betroffenen.
Menschen, die ein hohes Risiko für Lungenkrebs haben, könnten allerdings von Vorsorgeuntersuchungen profitieren. Es wurden zum Beispiel Studien durchgeführt, bei denen Risikopatienten regelmäßig mittels Computertomografie (CT) mit niedriger Strahlendosis untersucht wurden. Auf diese Weise konnte etwa bei starken Rauchern Bronchialkrebs früher entdeckt werden. Dies muss aber noch genauer untersucht werden. Erst dann kann man vielleicht solche Vorsorgeuntersuchungen für bestimmte Risikogruppen empfehlen.
Lungenkrebs: Krankheitsverlauf und Prognose
Für Patienten, die eine Therapie mit Heilungsabsicht (kurative Therapie) bekommen haben, gibt es einen speziellen Nachsorgeplan. Nach Abschluss der Behandlung sollten sie in regelmäßigen Abständen zu Kontrolluntersuchungen ins Krankenhaus gehen. Besonders wichtig sind regelmäßige Röntgen- und CT-Bilder. Der Arzt wird diese jeweils im Vergleich zu den letzten Aufnahmen des Patienten beurteilen.
Auch Patienten, bei denen keine Heilung mehr zu erwarten ist, werden regelmäßig vom Arzt untersucht. So lässt sich feststellen, ob die palliative Therapie die Symptome ausreichend lindert oder eventuell angepasst werden muss.
Lungenkrebs: Prognose
Insgesamt hat das Bronchialkarzinom eine schlechte Prognose: Lungenkrebs wird bei vielen Patienten erst entdeckt, wenn die Erkrankung bereits weit fortgeschritten ist. Eine Heilung ist dann oft nicht mehr möglich. Wird der Lungenkrebs in frühen Stadien entdeckt, kann man eventuell operieren. Nach einiger Zeit bildet sich aber oft ein erneuter Krebstumor (Rückfall = Rezidiv).
Gerade weil die Heilungschancen so gering sind, ist es wichtig, das Risiko für Lungenkrebs nicht unnötig zu erhöhen. Der wichtigste Faktor, den jeder selbst in der Hand hat, ist das Rauchen. Wer auf das Qualmen verzichtet oder gar nicht erst damit anfängt, senkt deutlich sein persönliches Risiko für ein Bronchialkarzinom. Prognose und Verlauf einer bereits bestehenden Lungenkrebs-Erkrankung lassen sich ebenfalls verbessern, wenn man mit dem Rauchen aufhört.
Lungenkrebs: Lebenserwartung
Wer die Diagnose Lungenkrebs bekommt, stellt sich oft die Frage: «Wie lange werde ich noch leben?» Für den Arzt ist es nicht ganz einfach, diese Frage zu beantworten. Die Lebenserwartung bei Lungenkrebs hängt nämlich von verschiedenen Faktoren ab:
Es spielt zum Beispiel eine Rolle, wie weit fortgeschritten der Tumor zum Zeitpunkt der Diagnose ist. Lungenkrebs wird oft erst spät entdeckt, was sich nachteilig auf die Lebenserwartung des Patienten auswirkt. Ebenfalls einen Einfluss auf das Überleben hat die Art des Tumors: Nicht-Kleinzellige Bronchialkarzinome wachsen langsamer als Kleinzellige. Sie haben deshalb generell eine bessere Prognose.
Der allgemeine Gesundheitszustand ist ebenfalls wichtig: Wenn zum Beispiel die Herz- und Lungenfunktion eines Patienten deutlich geschwächt sind, kann es sein, dass bestimmte Behandlungsformen nur eingeschränkt oder gar nicht durchgeführt werden können. Das kann die Lebenserwartung des Lungenkrebs-Patienten deutlich senken.
Nähere Informationen zu Lebenserwartung und Heilungschancen bei Lungenkrebs erfahren Sie im Text Lungenkrebs: Lebenserwartung.
Weiterführende Informationen:
retningslinjer:
- S3-Leitlinie «Prävention, Diagnostik, Therapie und Nachsorge des Lungenkarzinoms» der Arbeitsgemeinschaft der Wissenschaftlichen MedizinischenFachgesellschaften e.V., der Deutschen Krebsgesellschaft e.V. und der Deutschen Krebshilfe (2018)
Selbsthilfegruppen:
- Bundesverband Selbsthilfe Lungenkrebs e.V.
- Selbsthilfe Lungenkrebs
- Deutsche Krebshilfe e.V.